Informativo Técnico Nº. 187
A Pasteurella
Multocida Tipo A Atuaria Como Agente Primário nos
Processos Pneumônicos dos Suínos?
Autor :
Jalusa Deon Kich; Nelson Morés; Nelise Juliane Triques; Mariana Gomes Nogueira; Catiuscia Locatelli; Cátia Silene Klein; Rinaldo Perez FelícioIntrodução
A Pasteurella multocida tipo A (PmA) é citada na literatura como
agente secundário, principalmente ao Mycoplasma hyopneumoniae (Mhy) na pneumonia enzoótica. As dificuldades na reprodução experimental da
doença e na identificação de fatores de virulência levaram a esta conclusão.
Porém, tem sido observado problemas pneumônicos em alguns rebanhos brasileiros
com quadro patológico semelhante a pleuropneumia
suína (PPS) e doença de Glässer com isolamento
exclusivo de PmA na pesquisa bacteriológica. Para
esclarecer melhor estas observações, foi realizado a
reprodução experimental de casos clínicos por meio da inoculaçãol
de dois suínos livres de patógenos respiratórios (Specific Pathogen Free - SPF) e um suíno de sistema de criação convencional
com amostras de PmA.
Condução
do estudo e resultados
As amostras de PmA utilizadas neste estudo foram
isoladas de animais necropsiados em granja de ciclo
completo com 200 matrizes, onde estava ocorrendo o problema respiratório em
abril de
A granja foi
visitada para avaliação clínica e do manejo praticado. No
crescimento/terminação o principal sinal clínico observado foi tosse intensa,
dispnéia e respiração abdominal (batedeira) e lotes desuniformes. Quatro suínos
com sinais clínicos respiratórios foram necropsiados
para avaliação patológica e colheita de material para exames bacteriológico,
histopatológico e imunoistoquímica (IHQ). Na
necropsia as observações foram pneumonia muco-purulenta
comprometendo grandes áreas do pulmão (aproximadamente 60%) e pleurite difusa
com aderência entre as pleuras parietal e visceral.
Desses animais
foram isoladas quatro amostras com características morfológicas e bioquímicas
de PmA, sendo uma de suabe de pleura e três de pulmão oriunda de suínos
diferentes. No exame histopatológico foram observados severa exsudação muco-purulenta nos alvéolos, brônquios e brônquíolos, espessamento dos septos interlobulares
por edema, infiltração inflamatória mista, hemorragia e início de fibrose,
hiperplasia linfo-reticular peribronquial
e perivascular. O diagnóstico morfológico foi de broncopneumonia purulenta
subaguda. Na avaliação imunoistoquímica foi
encontrada reação positiva para Mhy no pulmão e, com
escassa quantidade de antígeno, para PCV2 nos linfonodos.
Reprodução
experimental da doença
Para reprodução
experimental da doença foram utilizadas três amostras de PmA isoladas dos suínos necropsiados.
Dessas, produzidos três inóculos a partir de amostras
cultivadas em agar DSA
(Dextrose Starch Agar) e suspensos em salina estéril
como segue:
- PmA1 - pool de três amostras
isoladas de lesões do pulmão (abril de 2007) contendo 2,6X107 UFC/mL;
- PmA2 - amostra isolada de lesões da
pleura (abril de 2007) contendo 2,1x108 UFC/mL;
- PmA3 - amostra fornecida pelo
Laboratório CEDISA, isolada anteriormente da mesma granja (março de 2007)
a partir de lesão hemorrágica do pulmão contendo 9,6x108 UFC/mL.
Inoculação: foram inoculados dois suínos SPF de 94 dias de idade, sendo
que o leitão 1 recebeu o inóculo PmA1
e o leitão 2 o inóculo PmA2. O terceiro leitão
inoculado (leitão 3) era de um sistema de criação convencional com 96 dias de
idade e recebeu o inóculo PmA3.
Cada leitão foi inoculado por instilação nasal 3,0 mL (1,5 mL em cada narina)
da suspensão correspondente.
Exames: foi realizado
avaliação macroscópica e microscópica das lesões e pesquisa bacteriológica dos
seguintes patógenos: Pasteurella
multocida, Actinobacillus pleuropneumoniae (App) e Haemophilus parasuis (Hps).
Leitão
1 - inoculado com a PmA1
Sinais
clínicos: o leitão apresentou polipnéia leve e febre, com temperatura retal de 41,0oC e 40,3oC,
24 e 48 horas após a inoculação, respectivamente. A necropsia foi realizada
dois dias após a inoculação.
Necropsia: observaram-se linfonodos
submandibulares e mediastínicos com leve aumento de
volume, edema interlobular e hepatização
vermelha em cerca de 70% do lobo cardíaco direito, o qual se apresentou
aumentado de volume em relação ao restante do parênquima. Na área hepatizada, a pleura pulmonar estava hiperêmica,
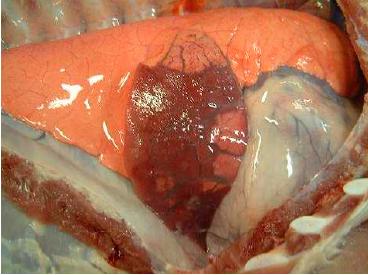
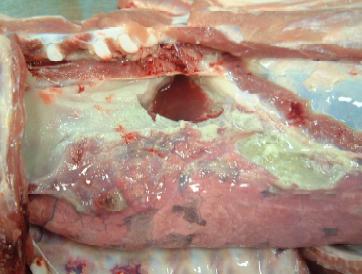
opaca, edematosa e com fina camada de fibrina na superfície (Fig.1). Havia leve
aumento na quantidade de líquido pleural e pericárdico, o qual apresentavase turvo e avermelhado, com grumos de fibrina.
Fig.1. Grande área de hepatização
pulmonar com edema interlobular e fina camada de
fibrina sobre a pleura, no lobo cardíaco esquerdo.
Histopatologia: O pulmão apresentava severa exsudação de fibrina, polimorfonucleares e edema no interior dos alvéolos, no
espaço interlobular, na região subpleural
e sobre a pleura; áreas de necrose coagulativa do
parênquima (Fig.2), com hemorragia, necrose fibrinóide
e trombose de vasos sanguíneos e linfáticos (Fig.3); severa exsudação de
neutrófilos na mucosa dos brônquios e bronquíolos, formando exsudato
muco-purulento no interior dessas estruturas; presença de muco e neutrófilos no
interior dos brônquios (Fig.4). A infiltração inflamatória era
predominantemente de neutrófilos (Fig.5). Os linfonodos
mediastínicos estavam hiperativos e com áreas de
acentuada infiltração de neutrófilos.
O diagnóstico
morfológico desse animal foi de broncopneumonia fibrino-necrótica
purulenta com pleurite fibrinosa.
Fig. 2. Necrose coagulativa do parênquima
pulmonar com edema e infiltração inflamatória (seta).
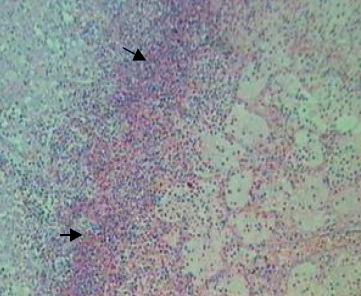
Fig. 3. Necrose hialina da parede de vaso sangüíneo (setas).
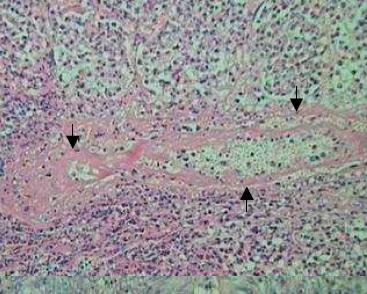
Fig. 4. Exsudação de neutrófilos pela mucosa bronquial e conteúdo
muco-purulento no interior.
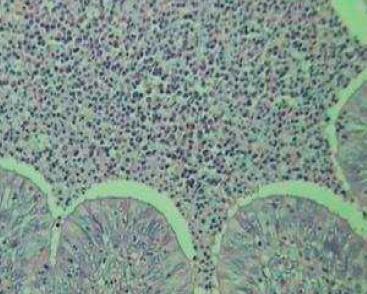
Fig.5. Exsudato intra-alveolar de fibrina e neutrófilos.
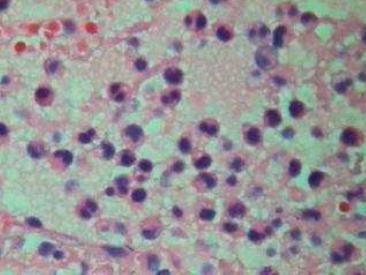
Bacteriologia: foi isolada uma amostra com características morfológicas e
bioquímicas de PmA a partir
de pulmão e não foram isoladas amostras suspeitas de App
e Hps.
Leitão
2 - inoculado com a PmA2
Sinais
clínicos: observaram-se febre, com
temperatura retal de 40,5oC
e 40,0oC, 24 horas e 5 dias após a inoculação,
respectivamente, anorexia e emagrecimento progressivo durante cinco dias de
observação pós-inoculação, quando foi realizada a necropsia.
Necropsia: observou-se presença de grande quantidade de líquido cítrico
contendo fibrina em fase de organização nas cavidades pleurais, provocando
aderência frouxa da pleura visceral com a parietal (Fig.6). No pericárdio havia
espessa e difusa camada de fibrina amarelada provocando aderência frouxa entre epicárdio e pericárdio (Fig.7 e 8). Sobre o diafragma
pulmonar e lobos cardíacos e apicais, também havia espessa camada de fibrina
amarelada em fase de organização. Na região antero-ventral e em algumas áreas dos lobos diafragmáticos
do pulmão havia hepatização vermelha. Havia um nódulo
de necrose fibrinohemorrágico na face dorsal do lobo
diafragmático com pleurite, semelhante a lesão de PPS
(Fig.9).
Fig. 6. Hepatização
nos lobos cardíaco e diafragmático (setas) e grande quantidade de liquido na
cavidade pleural.
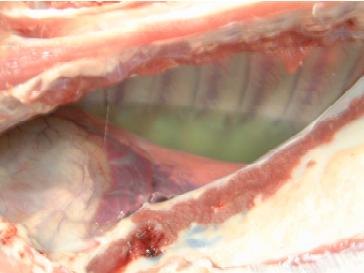
Fig. 7. Severa exsudação de fibrina no saco pericárdico
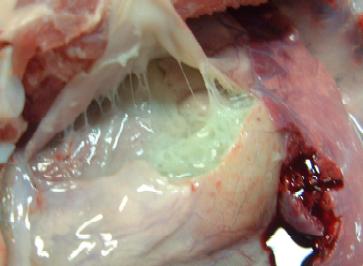
Fig. 8. Severa e difusa deposição de fibrina no epicárdio.
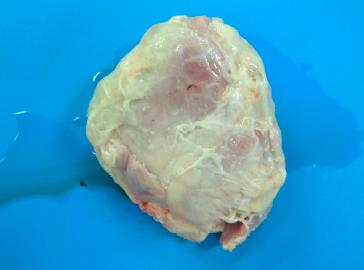
Fig. 9. Difusa deposição de fibrina sobre a pleura (setas), exsudado
serofibrinoso na cavidade pleural e área irregular de
pneumonia necrohemorrágica (círculo)-lesão App like.
Histopatologia: no pulmão as lesões eram semelhantes ao leitão 1, porém, com
início de fibroplasia a partir da pleura, septos interlobulares e periferia de vasos sanguíneos e brônquios.
Havia acentuada exsudação de fibrina e neutrófilos sobre a
pleura (Fig.10). As áreas de necrose eram irregulares, melhor definidas,
e com tentativa de encapsulamento por tecido fibroso,
assemelhando-se àquelas da PPS (2), porém com infiltrado inflamatório
predominantemente de neutrófilos (Fig.11). O coração apresentava severa
deposição de fibrina no epicárdio, mesclada com células
inflamatórias, edema e início de fibroplasia
caracterizando pericardite fibrinosa difusa. O
sistema linfóide estava hiperativo com infiltração de neutrófilos,
especialmente na periferia, e haviam áreas de
hemorragia nos seios subcapsulares.
O diagnóstico
morfológico desse animal também foi de broncopneumonia fibrino-necrótica
purulenta com pleurite fibrinosa. Comparativamente,
em relação ao suíno 1, as lesões de exudação fibrinosa foram muito mais extensas e evoluindo para a
cronicidade neste animal.
Fig. 10. Exsudação de fibrina e
células inflamatórias sobre a pleura
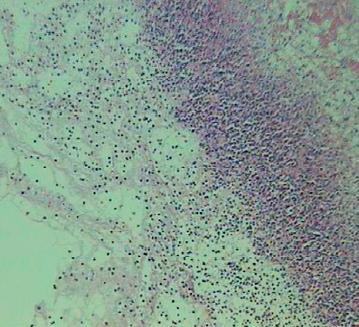
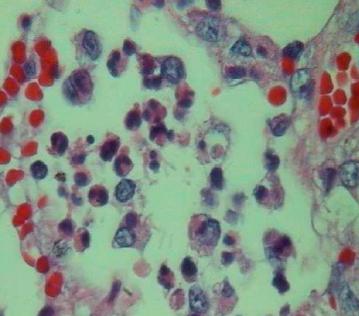
Fig. 11. Exsudação
intra-alveolar de neutrófilos e macrófagos alveolares.
Bacteriologia: isolamento de amostra com características morfológicas e
bioquímicas de PmA a partir
da superfície externa do pulmão numa área de aderência da pleura e não foram
isoladas amostras suspeitas de App e Hps.
Leitão
3 – inoculado com a PmA3
Sinais
clínicos: o leitão estava
ofegante, mantendose em decúbito ventral sem se
alimentar de
Necropsia: Na região antero-ventral do pulmão e em
algumas áreas dos lobos diafragmáticos havia hepatização
vermelha e aderência entre lobos; sobre a pleura havia fibrina amarelada em
fase de organização, assemelhando-se a material purulento provocando aderência
frouxa das pleuras visceral e parietal (Fig.12). No pericárdio e no peritônio
(Fig.13) também havia presença de fibrina. Desse animal não foi realizado exame
histopatológico, porém o diagnóstico de necrópsia foi
lesões agudas de broncopneumonia purulenta com poliserosite,
envolvendo inclusive o peritôneo.
Fig.
12. Áreas de hepatização disseminadas no pulmão e deposição de fibrina
sobre a pleura.
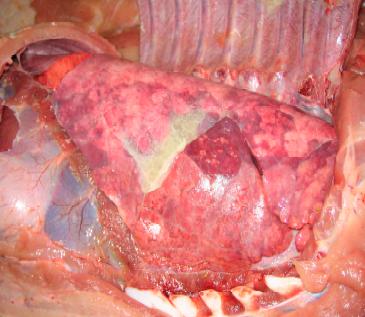
Fig. 13. Filetes de fibrina
sobre as visceras abdominais.
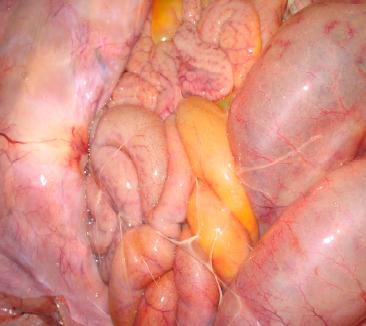
Bacteriológico: foi isolada amostra
com características morfológicas e bioquímicas de PmA a partir de suabe de
pleura, peritônio e líquido do pericárdio e não foram isoladas amostras
suspeitas de App e Hps.
Discussão
As lesões
encontradas nos suínos inoculados caracterizaram um quadro morfológico de pleuropneumonia purulenta necro-hemorrágica
e fibrinosa, no suíno 1, e subaguda no 2, com isolamento em cultivo puro de PmA
a partir das lesões pulmonares e de serosas. O suíno 3 apresentou lesões
macroscópicas de broncopneumonia purulenta com lesões de poliserosite
semelhantes a Doença de Glässer,
porém com isolamento em cultivo puro de PmA e
negativo para Hps. A pesquisa bacteriológica foi
realizada a partir da fibrina depositada nas cavidades torácica, abdominal
(Fig.12 e 13) e líquido do pericárdio. As lesões macroscópicas observadas no
animal 2 foram semelhantes àquelas encontradas na PPS por Actinobacillus
pleuropneumonia (2), exceto o tipo de exsudato/infiltrado inflamatório que nesse caso foi
predominantemente de neutrófilos, o que tem sido citado nos casos de pasteurelose subaguda (3). Embora a carga bacteriana de PmA utilizada nas inoculações
tenha sido bastante elevada, ficou evidente que as cepas foram capazes de induzir
quadros clínicos e lesões severas de doenças respiratórias em apenas 24 horas.
A PmA tem sido relatada como
um agente que interage diretamente com muitos agentes respiratórios,
especialmente o Mhy (3), mas nesse caso em
inoculações de suínos livres de patógenos
respiratórios (suínos 1385 e 1378), as amostras utilizadas comportaram-se como
agentes primário no desenvolvimento do quadro patológico. Existe um debate na
literatura sobre o papel da PmA
como agente secundário ou primário, baseado em insucessos com a reprodução
experimental da doença e variabilidade nos estudos de fatores de virulência
(3). Isto pode ser atribuído ao isolamento de amostras não patogênicas
presentes no sistema respiratório de suínos sadios. Os resultados aqui
observados indicam que existem amostras de PmA que por si só são capazes de induzir a doença e
que são boas candidatas a futuros estudos de fatores de virulência.
Comentários
e recomendações
Alerta-se que
no diagnóstico de problemas respiratórios agudos em suínos em fase de
crescimento-terminação amostras de PmA
podem ser consideradas como agente primário das lesões.
As lesões
macroscópicas provocadas por amostras de PmA,
podem ser confundidas com àquelas causadas por amostras de App
ou Hps. Por esta razão, tais lesões devem ser
submetidas a exames laboratoriais para confirmação do diagnóstico incluindo a
pesquisa de PmA como
possível agente primário.