Informativo Técnico Nº. 242
DOENÇA DE GLASSER
INTRODUÇÃO
Inúmeros microorganismos, alguns potencialmente patogênicos,
colonizam suínos já nas primeiras horas de vida. Um destes agentes é o Haemophilus parasuis
(HP), que tem sido associado à doença de Glasser em
suínos desde 1910.
A doença de Glasser é uma síndrome
bem definida, caracterizada por serosites, envolvendo
a pleura, pericárdio, peritônio e também está associada à meningite, artrite
e pneumonia serofibrinosa. Antigamente, esta
síndrome ocorria nas granjas esporadicamente, acometendo suínos jovens,
associada a fatores estressantes como desmame,
transporte ou presença de outras doenças respiratórias primárias. Entretanto,
atualmente, nas propriedades de alto "status" sanitário, livres do
HP, quando ocorre exposição ao referido patógeno pode
ocorrer doença sistêmica sem que haja fatores estressantes envolvidos.
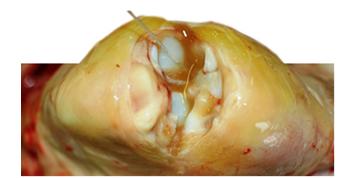
Figura 1: Artrite causada por Haemophilus parasuis.
Fonte: Retirado do site pig333.
A interação entre HP e alguns agentes virais como o vírus da
Síndrome Reprodutivo-Respiratório (PRRSV), da Doença de Aujezsky
e Circovírus Suíno tipo 2 (PCV2) tem sido relatada.
Embora ainda não tenha sido estabelecida uma associação direta entre esses agentes
virais e o HP, observações a campo têm indicado que a mortalidade causada pelo
agente pode aumentar quando há uma infecção ativa na granja, particularmente no
caso do vírus da PRRS.
São descritos até o momento 15 sorotipos, supostamente,
baseados na heterogenicidade da cápsula ou camada de lipopolissacarídeo (LPS). No Brasil, analisando amostras
provenientes de 204 granjas de suínos de diferentes estados do país,
pesquisadores obtiveram 321 isolados de HP, sendo que os sorotipos 1, 4, 5 e 12
foram os mais prevalentes. Dados similares são descritos em outros países.
EPIDEMIOLOGIA
Até o momento não se sabe do processo infeccioso Haemophilus parasuis em
outras espécies, apenas suinos. Em granjas
convencionais é a primeira bactéria isolada de suabes
nasais de leitões com uma semana de vida e a mais prevalente. Tem sido isolado
com freqüência de secreções nasais de suínos sadios e de pulmões de suínos com
pneumonia, mas geralmente não há isolamento de pulmões normais.
O trato respiratório superior de suínos sadios é colonizado
por duas sub-populações de HP, que diferem nas
características fenotípicas e genotípicas. Isolados de HP não patogênicos são
altamente prevalentes no trato respiratório superior de porcas, colonizando-o
rapidamente, enquanto que isolados potencialmente patogênicos disseminam-se
mais lentamente, devido, provavelmente, a sua baixa prevalência nesses animais.
A infecção sistêmica dos animais precocemente colonizados é prevenida pela
presença dos anticorpos maternos, que podem permanecer até
Leitões desmamados podem ser infectados por diferentes
amostras de HP (patogênicas ou não). No caso das amostras patogênicas, os
animais infectados tornam-se portadores sadios, podendo ser fonte ativa de
infecção para os suscetíveis na creche. Embora haja uma grande diversidade de
isolados de HP em leitões desmamados provenientes de diferentes sítios, 2 ou 3
amostras prevalecerão em granjas infectadas, permanecendo estáveis no rebanho
até um ano.
APRESENTAÇÕES CLÍNICAS
O HP tem
sido associado a 3 principais quadros clínicos afetando, normalmente, os
melhores leitões:
1) O
primeiro se caracteriza por uma serosite generalizada
(forma clássica da Doença de Glasser);
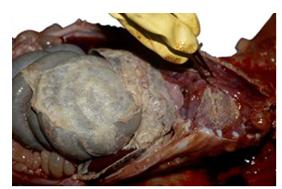
Figura 2: Presença visível de
fibrina na cavidade peritoneal (peritonite fibrinosa)
e cavidade pericárdica (pericardite fibrinosa).
Fonte: Retirado do site pig333.
2) O segundo está associado a uma
septicemia, sem poliserosite, podendo ocorrer mortes
súbitas, sendo que alguns suínos podem apresentar a forma clássica da Doença de
Glasser;
3) O terceiro quadro cursa com
pneumonia (casos de broncopneumonia supurativa, onde o HP atua como agente
primário ou, mais freqüentemente, secundário).
DIAGNÓSTICO
O diagnóstico presuntivo de HP é baseado no histórico,
sinais clínicos e lesões observadas à necropsia, e sua confirmação estabelecida
por meio de seu isolamento, o qual nem sempre resulta positivo. Isso se
deve ao fato do agente requerer condições especiais para o seu crescimento,
além da possibilidade do HP estar presente em baixo número nos órgãos e
líquidos e ao fato dos animais terem sido submetidos à
antibioticoterapia.
Para aumentar as chances de diagnóstico realiza-se o cultivo
dos órgãos com lesões serofibrinosas, como pulmão,
cérebro e meninge, líquido pericárdico e sinovial,
onde culturas puras de HP podem ser observadas após 48 horas de incubação a
37ºC. Outras metodologias diagnósticas têm sido desenvolvidas, mas restritas a
alguns centros ou laboratórios de referência, como o teste de ELISA, imunufluorescência, imuno-histoquímica
e hibridização.
CONTROLE
Diferentes estratégias de controle têm sido propostas,
dependendo da dinâmica da infecção pelo HP em cada granja. Em algumas
situações, especialmente quando a doença é de ocorrência esporádica, o
tratamento com antimicrobianos tem sido usado. Porém, em surtos severos, a antibioticoterapia não tem sido efetiva em reduzir os
sinais clínicos e mortalidade, sendo indicado o uso de vacina.
Além das vacinas comerciais, bacterinas
autógenas também têm sido usadas. Estas são produzidas com amostras
recuperadas de animais infectados pelo HP. Porém, é importante salientar a
necessidade de colher vários órgãos dos animais durante a fase aguda e submeter
ao exame bacteriológico (COD. S51- BACTERIOLOGIA SISTEMA RESPIRATÓRIO),
para verificar a possibilidade da existência de mais de um sorotipo na granja,
ou mesmo no animal e incluí-las na vacina. A demonstração de proteção
cruzada entre os sorotipos de HP tem sido esporádica e inconsistente, restrita
a alguns sorotipos.
Tem sido demonstrado que a proteção das vacinas comerciais
falha quando usada em propriedades onde as amostras prevalentes diferem
daquelas incluídas na vacina. Nesses casos, vacinas autógenas têm sido
usadas para reduzir a mortalidade.
O esquema de vacinação mais comum indicado para a prevenção
da doença consiste na imunização dos leitões antes do desmame. Freqüentemente
são indicadas duas doses, uma aos sete dias de idade e outra no desmame.
Entretanto, em granjas onde a doença de Glasser ocorre
em leitões muito jovens, é indicada a vacinação das porcas na gestação. Nesse
caso, a imunidade passiva, através dos anticorpos maternos, pode minimizar os
efeitos da doença nas primeiras três a cinco semanas de vida dos
leitões. Quando a vacinação das porcas é também utilizada, os leitões devem ser
vacinados mais tarde para proporcionar uma imunidade ativa mais prolongada.
Os programas de controle também devem incluir práticas
adequadas de manejo, visando a reduzir ou eliminar outros patógenos
respiratórios, uniformização da idade do desmame, eliminação da mistura de
suínos de diferentes idades e outros fatores de estresse.
Referência: Texto compilado do site
da Associação Brasileira dos Criadores de Suíno (http://www.abcs.org.br/)
|
CODIGO |
EXAMES |
PRAZO DIAS |
|
S51 |
BACTERIOLOGIA
SISTEMA RESPIRATÓRIO Material:
Swabs nasais, de pulmão e tonsilas; Pesquisa:
Actinobacillus pleuropneumoniae,
Bordetella bronchseptica,
Haemophillus parasuis, Pasteurella multocida e antibiogramas. |
5 |
|
S16 |
ISOLAMENTO
- Streptococcus suis Amostra: Swab nasal,
tonsilas e sistema nervoso central |
5 |
|
S56 |
APP -
MÉTODO ELISA Amostra: Soro |
3 |
|
S64 |
Bordetella bronchiseptica Amostra: Soro |
2 |
|
S05 |
PMT - Pasteurella multocida
TOXIGÊNICA Amostra: Soro |
2 |
|
S08 |
Mycoplasma hyopneumoniae - MH KIT IDEXX Amostra:
Soro
|
3 |
|
S06 |
PRRS –
ELISA Amostra: Soro |
3 |
|
BIO |
HISTOPATOLOGIA
– BIOPSIA Amostra: Fragmento de órgão em formol 10% |
5 |
|
V20 |
VACINA AUTÓGENA CONTRA
ESTREPTOCOCOSE DOS SUÍNOS E HPS Amostra: Cepas isoladas na propriedade. |
15 |