Informativo Técnico Nº. 267
Medicamentos e medicações no controle de doenças entéricas pós-desmame
Autor/s. : Ton
Kramer, Médico-veterinário, Gerente Comercial de Suínos.
Introdução
Nos últimos 40 anos, a
suinocultura brasileira
passou por grandes transformações. Manejo,
instalações, nutrição, genética e
sanidade evoluíram de tal forma que há alguns anos o
Brasil tornou-se
referência na produção de suínos. Com o
aumento da própria produção e da
produtividade, os desafios sanitários cresceram
proporcionalmente, resultado da
intensificação e da concentração da
produção em determinadas regiões do país.
Decorrente disso e da busca inconstante pelos melhores resultados
zootécnicos e
financeiros, o uso de promotores de crescimento e aditivos alimentares
passou a
ser rotineiro.
A eleição do medicamento ou
programa medicamentoso vai depender do agente etiológico envolvido e a fase que
acomete o animal

O início dos anos 2000 foi marcado pelos
crescentes casos de circovirose e das doenças
associadas. Durante esse período, entre as diversas medidas de manejo adotadas
no intuito de minimizar os prejuízos, como os reconhecidos 20 Pontos de Madec, o uso de programas medicamentosos, alternando pulsos
antibióticos com períodos de uso contínuo, foi uma estratégia positiva no
sentido de frear o impacto negativo da síndrome.
Com o advento das diversas opções de vacinas
contra a circovirose e a melhoria nas práticas de
manejo, os desafios sanitários diminuíram e, por consequência,
o uso dos programas medicamentosos.
No entanto, ao longo de todo esse período, a
pressão econômica promoveu alguns abusos no uso de medicamentos, especialmente
antibióticos, que, por vezes, foram utilizados em subdosagens
por períodos menores ao prescrito pelo médico-veterinário ou recomendado pelo
laboratório farmacêutico, ou, ainda, pelo uso de drogas-padrão como matériaprima.
Do outro lado da cadeia de produção, o consumidor
passou a ser cada vez mais exigente. Da mesma forma, e uma vez que o Brasil
passou a ser um importante exportador de carne suína, os países importadores
passaram a ser mais exigentes. Como resultado disto, restrições foram impostas
ao uso de medicamentos. Some-se a isso, ainda, uma preocupação cada vez maior
da área médica no que diz respeito às resistências bacterianas e as discussões
ainda inconclusivas da importância que a produção animal tem neste processo,
decorrente do uso dos aditivos alimentares melhoradores
de desempenho.
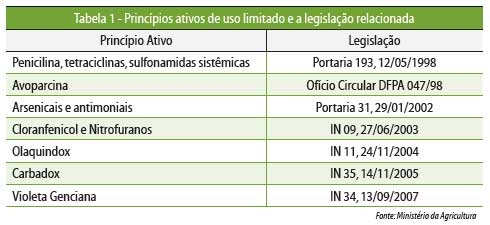

Em 1986, o Ministério da Agricultura brasileiro
lançou o Plano Nacional de Controle de Resíduos (Portaria n° 51, de 6 de
fevereiro de 1986). Como resultado deste plano, em 1999 foram
lançados os Programas de Controle de Resíduos em Carne (Portaria n° 42, de 20
de dezembro de 1999). Paralelamente, foi restringido ao longo dos anos o uso de
alguns princípios ativos, relacionados na Tabela 1.
Mais recentemente, outras instruções normativas
foram publicadas no sentido de normatizar e regular a importação, fabricação,
comercialização e uso de medicamentos, sendo:
- Instrução Normativa nº 13,
de 30 de novembro de 2004: aprova o regulamento técnico sobre aditivos
para produtos destinados à alimentação animal;
- Instrução Normativa nº 65,
de 21 de novembro de 2006: aprova os
procedimentos para a fabricação e o emprego de rações, suplementos, premixes, núcleos ou concentrados com medicamentos
para os animais de produção;
- Instrução Normativa nº 04,
de 23 de fevereiro de 2007: aprova o regulamento técnico sobre as
condições higiênico- sanitárias e de boas práticas de fabricação para
estabelecimentos fabricantes de produtos destinados à alimentação animal e
o roteiro de inspeção;
- Instrução Normativa SDA nº
29, de 14 de junho de 2007: aprova os procedimentos para a importação de
produtos destinados à alimentação animal;
Além disso, está em discussão o
Relatório Técnico do Grupo de Trabalho instituído pela Portaria SDA nº 428, de
10 de dezembro de 2009, que "sugere descontinuidade do uso como aditivo melhorador de desempenho por preocupações relacionadas à
saúde pública" (Ofício nº 087/2011/DFIP, de 10 de maio de 2011),
especialmente, em relação à segurança toxicológica, os princípios ativos clorexidina, halquinol, e em
relação ao desenvolvimento de resistência bacteriana, os princípios ativos espiramicina, eritromicina, tiamulina, lincomicina e colistina.
Todas essas ações têm como intuito ou consequência:
- Definir os princípios
ativos passíveis de uso em medicina veterinária e que não resultem em
possível resistência bacteriana a medicamentos de uso na medicina humana;
- Garantir origem, qualidade
e destino dos aditivos e medicamentos utilizados na produção animal;
- Valorizar o profissional
da área médica veterinária no sentido de prescrever e recomendar o uso de
medicamentos com base em um diagnóstico;
- Diferenciar o uso dos
antibióticos como terapêuticos e aditivos melhoradores
de desempenho.
Princípios gerais no uso de antibióticos
O uso de um antibiótico na produção animal tem
objetivos que vão além do simples tratamento de uma infecção ou desafio
bacteriano (Tabela 2).
Figura 1 - Princípios
da escolha do antibiótico
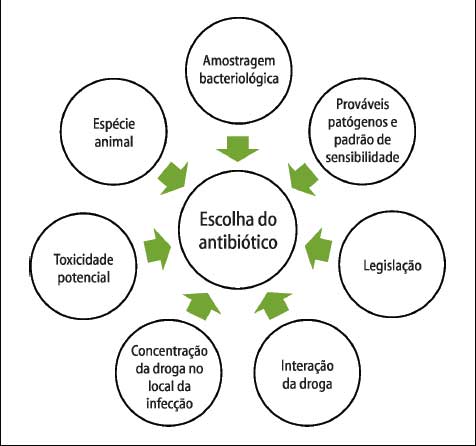
A escolha de um medicamento ou programa
medicamentoso depende das informações disponíveis no momento. No entanto,
devem-se levar em consideração os aspectos da Figura 1.
Os tratamentos antibióticos
Estando determinados os contextos clínico,
econômico e sanitário e tendo o diagnóstico definido, pode-se estabelecer o
tratamento a ser realizado.
De maneira geral, os tratamentos antibióticos
podem ser diferenciados em terapêutico (ou curativo) e
profilático (ou preventivo).
Um tratamento antibiótico terapêutico é
normalmente administrado para um grupo de animais que apresentem os sinais
clínicos da doença, ou em todo o lote, quando houver a expectativa de que
outros animais possam desenvolver a infecção. O objetivo deste tipo de
tratamento é eliminar o microrganismo causador da infecção, seja de manifestação
clínica, subclínica ou assintomática.
O tratamento profilático (ou preventivo), por sua
vez, é normalmente utilizado quando há uma grande probabilidade da infecção
bacteriana no lote, e o tratamento terapêutico, por sua vez, no caso da
manifestação clínica, é difícil ou de custo mais elevado.
Em uma visão médica, os tratamentos terapêuticos
deveriam ser os de preferência, especialmente aqueles direcionados
especificamente aos animais acometidos pela infecção. Isto porque o uso
preventivo é o primeiro passo para o uso sistemático, prática que pode ser
negativa, uma vez que pode levar ao desenvolvimento de resistência bacteriana e
é normalmente implementado para compensar um mau
manejo sanitário da granja.
Os princípios ativos e seus usos
O termo antibiótico (do grego anti =
contra e bio = vida) foi inicialmente
empregado para definir substâncias químicas produzidas por microrganismos que
têm a capacidade de, em pequenas doses, inibir o crescimento ou destruir
microrganismos causadores de doenças. Posteriormente, houve necessidade de
ampliar este conceito, pois se tornou possível obtê-los por síntese
laboratorial parcial (antibióticos semissintéticos ou
biossintéticos) ou total (sintobióticos)
(SPINOSA et al, 2005).
Os antibióticos podem ser classificados segundo:
- Estrutura química / Grupo
farmacológico
- Origem / Síntese
- Ação biológica
- Espectro de ação
- Mecanismo de ação
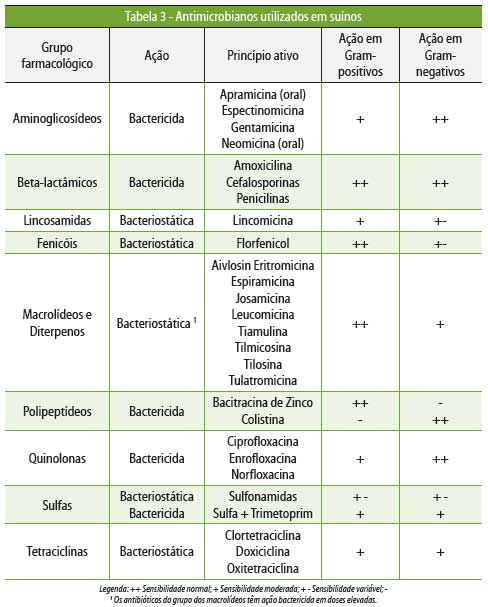
A Tabela 3 relaciona os principais antibióticos
utilizados na suinocultura brasileira e sua classificação.
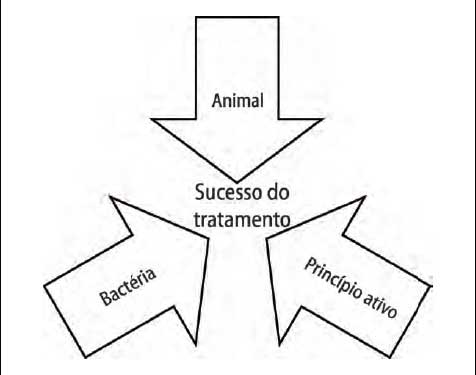
Considerando que o sucesso do tratamento
antibiótico é uma consequência da relação
"Animal - Bactéria - Princípio ativo" (Figura 2), quando da escolha
de um antibiótico ou associação de antibióticos, deve-se preferencialmente
conhecer o agente etiológico da doença. Quando isso não é possível, a escolha
do medicamento a ser utilizado deve considerar o quadro clínico, achados de
necropsia, epidemiológicos e laboratoriais, localização do processo infeccioso
e idade dos animais acometidos.
É importante ressaltar que os antibióticos nunca
eliminam a população bacteriana em sua totalidade: o crescimento bacteriano é
simplesmente interrompido (efeito bacteriostático) ou a população bacteriana é
reduzida a um nível mínimo (efeito bactericida). É sempre o sistema imune do
indivíduo que promove a completa eliminação da população bacteriana.
Figura 2 - Tríade de
envolvidos no tratamento medicamentoso
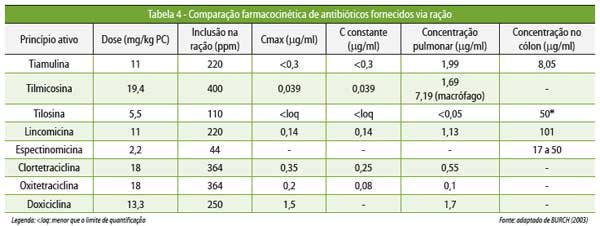
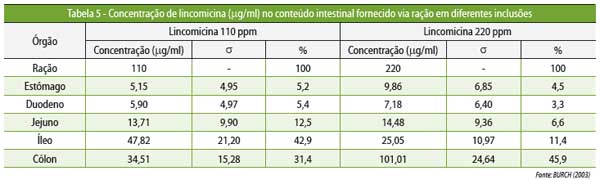
A análise da atividade antibacteriana deve considerar,
em um primeiro momento, o espectro de ação do medicamento e a concentração
inibitória mínima (CIM) para a bactéria que se quer combater. Na sequência, é necessário compreender as características
farmacocinéticas: o perfil farmacocinético para o tipo de processo infeccioso e
a CIM do antibiótico nos tecidos, uma vez que cada princípio ativo e tecido tem
um comportamento diferente (Figura 4 e Tabelas 4 e 5).
Quando um antibiótico é administrado em um
animal, a concentração do princípio ativo alcançada depende da farmacocinética
(metabolismo do animal). Os processos de absorção, distribuição e eliminação
determinam o perfil farmacocinético de um antibiótico (Figura 3).
Para agir nos órgãos-alvo, o antibiótico deve
ingressar na circulação (absorção) para então ser transferido pelo corpo
(distribuição). Uma vez na circulação, o comportamento do antibiótico é o
mesmo, independentemente da via de administração.
No entanto, a via de administração tem relação
direta para o tempo que o medicamento leva para alcançar a concentração máxima
no órgão-alvo. Considerando que na suinocultura as principais vias de
administração de medicamentos são injetáveis, via ração e água de bebida, de
acordo com o desafio apresentado, uma via terá preferência em relação às
demais. A Tabela 6 faz um comparativo entre as vantagens e desvantagens de cada
via.
Não há uma via de administração de medicamentos
única e ideal. Para cada infecção, uma via de administração será preferencial.
Devem ser considerados, para tanto, os recursos disponíveis, tanto de mão de
obra quanto equipamento, e as condições clínica dos animais. Além disso,
independentemente da via de administração utilizada para o tratamento, é
fundamental que as doses recomendas pelo fabricante do medicamento ou pela
literatura científica sejam respeitadas. O termo dosagem refere-se não somente
à dose diária individual de cada produto (normalmente expressa em mg de princípio ativo/kg de peso
corporal), mas também ao regime de administração (duração do tratamento e
intervalo entre as aplicações).
A dosagem utilizada de um antibiótico deve ser
suficiente para reduzir a população bacteriana de tal forma que o sistema imune
possa agir no sentido de eliminar a infecção. De acordo com a farmacologia
clássica, a dosagem ideal é aquela que garante uma concentração nos tecidos
mantém-se superior à CIM da bactéria, durante todo o período de tratamento. Em
casos em que há necessidade de um tratamento com antibióticos de ação
bactericida, os objetivos de concentração são muito mais altos que a CIM,
devendo superar a concentração bactericida mínima (CBM).
Figura 3 - Perfil
farmacocinético de um antibiótico administrado por diferentes vias
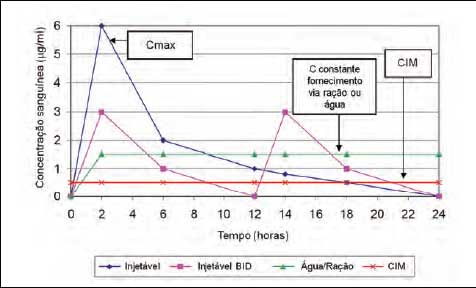
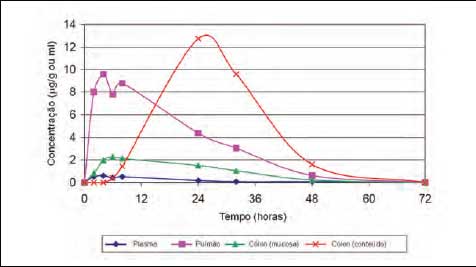
Figura 4 - Concentração
de tiamulina no plasma, pulmão e cólon, após a
aplicação injetável na dose de 15 mg/kg
de peso corporal (McKELLAR, 1993, citado por BURCH,
2003)
A dosagem indicada pelo laboratório farmacêutico
normalmente corresponde com aquela que é efetiva para o tratamento indicado e aprovada pelos órgãos reguladores competentes. No
entanto, essa dosagem não pode ser fixa, pelas diversas razões relacionadas com
a farmacologia. O médico-veterinário deve ser capaz de adaptar a dosagem, se
necessário, com base nas informações e dados disponíveis: CIM, concentração nos
tecidos, modo de ação dose ou tempo-dependente, disponibilidade de princípios
ativos, etc.
Outro ponto fundamental a ser considerado no que
diz respeito às dosagens tem a ver com a administração do medicamento,
principalmente via ração, quando normalmente as indicações estão descritas em ppm, ou seja, relacionadas com a
inclusão do produto na ração, sem levar em consideração a variação de consumo
ao longo da vida do animal.
A Tabela 7 mostra a dose diária e a inclusão na
ração recomendada para um medicamento, como a tiamulina,
cuja dose é 10 mg/kg, e com
uma apresentação comercial a 80%.
Combinação de antibióticos
A combinação de antibióticos tem como objetivo
aumentar a atividade antibiótica dos princípios ativos quando comparados aos
mesmos se usados individualmente, pela sinergia entre eles ou pelo aumento do
espectro de ação.
Além disso, a associação de antibióticos pode ter
a finalidade de evitar a possibilidade de resistência ou para atingir
diferentes locais de infecção.
É importante analisar o efeito da combinação
antes de empregá-la. Os efeitos da associação podem ser:
- Sinérgica: quando ocorre a potencialização do efeito esperado dos medicamentos.
Nesse caso, o efeito final é maior do que a soma dos efeitos de cada
antibiótico;
- Antagônico: quando o efeito
obtido é menor do que o esperado para cada um dos antibióticos ou, ainda,
há efeito tóxico;
- Indiferente: quando o
efeito dos antibióticos é independente, como se cada um deles estivesse
sendo utilizado isoladamente.
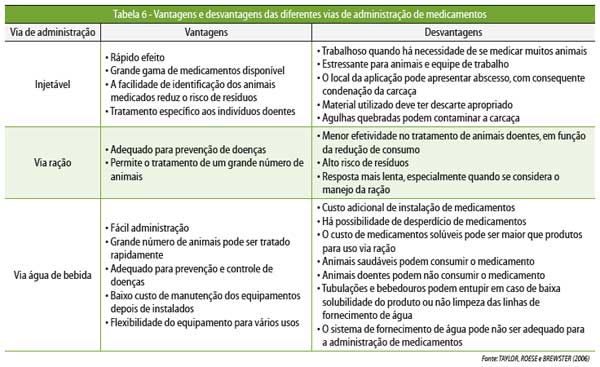
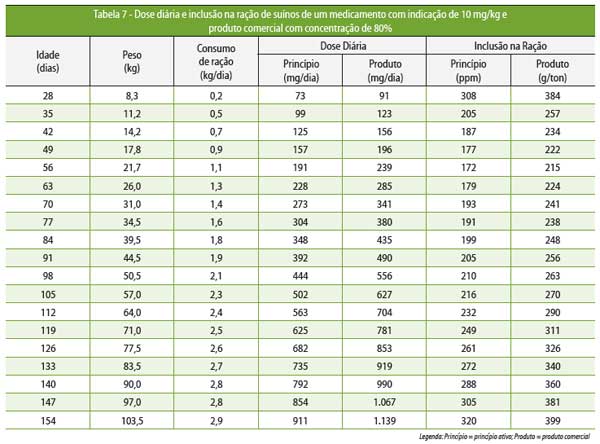
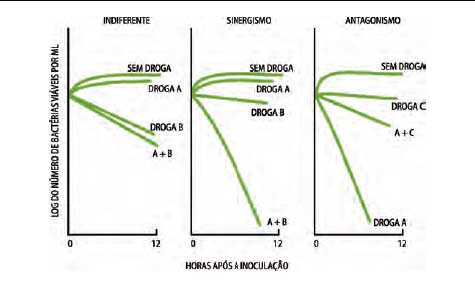
Figura 5 - Possíveis
efeitos da associação de antibióticos (SMITH e JAWETZ, 1972)
As regras gerais de associação de antibióticos
foram descritas por JAWETZ (1967), e são ainda válidas - Figura 5 (normalmente,
a associação entre antibióticos bacteriostáticos e bactericidas está
relacionada à fase do crescimento bacteriano - Figura 6):
- Combinação de dois
antibióticos bactericidas: pode ter uma ação sinérgica; é frequentemente indiferente;
- Combinação de dois
antibióticos bacteriostáticos: normalmente indiferente;
- Combinação de um
antibiótico bacteriostático com um bactericida cuja ação se dá na fase lag/de latência (aminoglicosídeos,
colistina e fluoroquinolonas):
normalmente indiferença;
- Combinação de um
antibiótico bacteriostático com um bactericida cuja ação se dá na fase
exponencial/de multiplicação (beta-lactâmicos):
normalmente antagonismo.
É importante ressaltar que estas regras têm
exceções relacionadas aos microrganismos e aos órgãos acometidos.
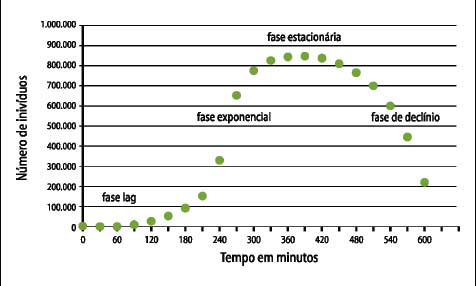
Figura 6 - Padrão de
crescimento bacteriano em um sistema fechado
Antibiogramas como ferramenta de escolha
do melhor tratamento
Embora o conceito e a técnica da realização de
antibiogramas sejam bastante simples, observam-se no dia a
dia dificuldades na interpretação e uso dos dados obtidos por esta
análise.
O antibiograma tem relevância no processo de
escolha de um tratamento antibiótico quando:
- O tempo gasto para a
execução do exame laboratorial e a obtenção do resultado é compatível com
a evolução da doença;
- O exame laboratorial
reflete a situação do campo.
Para tanto, a amostra de material utilizada para
a realização do antibiograma deve ser patologicamente representativa,
compatível com a história clínica da doença e sem fatores que possam interferir
negativamente no resultado do exame.
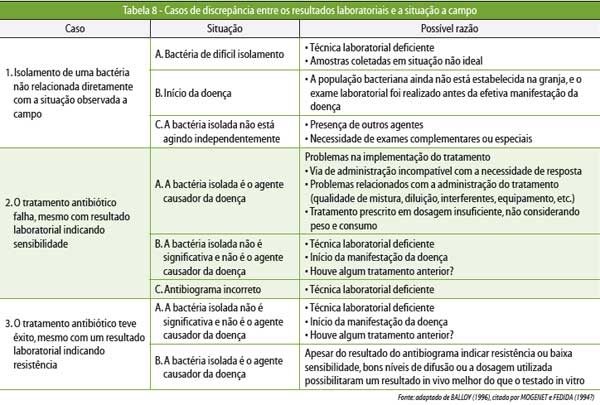
A Tabela 8 mostra os casos de discrepância entre
os resultados laboratoriais e a realidade a campo.
Resistência bacteriana
Define-se como resistência bacteriana a situação
em que é impossível obter-se a CIM. A consequência
disto é a falha no tratamento. No entanto, não necessariamente a falha no
tratamento seja sinônimo de resistência bacteriana.
O desenvolvimento de resistência bacteriana, além
de determinar menor eficácia da droga, também representa um potencial de risco
à saúde pública, uma vez que o contato dos homens com os animais pode aumentar
a ocorrência de resistência da microbiota desta
espécie (BONGERS et al, 1995, citado por BACCARO et al, 2002).
A resistência bacteriana pode ser:
- Intrínseca ou Natural:
quando a bactéria é naturalmente resistente a determinado princípio ativo;
- Adquirida: quando a
bactéria sofre uma mutação genética, que a permite sobreviver ou resistir
na presença de uma concentração de antibiótico superior ao usual. Essa
mutação pode ser resultado de uma alteração cromossômica ou extracromossômica (plasmídeo
ou transposon);
- Fenotípica ou Antibiotípica: quando uma cepa bacteriana é resistente
a um grupo antibiótico.
A ocorrência de resistência bacteriana está
relacionada com a prática rotineira de administração de tratamentos
antibióticos via oral, especialmente quando em subdosagens
ou por períodos menores do que o recomendado. Além disso, mudanças frequentes de moléculas, sem a avaliação da sensibilidade
bacteriana, ou, ainda, a mistura de diferentes antibióticos e a subdosagem são excelentes meios de promover o
desenvolvimento da resistência bacteriana.
As subdosagens resultam
em concentrações baixas do princípio ativo no organismo do animal, que não são
suficientes para inibir ou promover a eliminação bacteriana. Essa prática é
bastante comum, especialmente quando não são considerados o peso e o consumo
dos animais que estão sendo tratados (Tabela 7) e, muitas vezes, está
relacionada com o alto custo do medicamento utilizado.
O controle do desenvolvimento de resistência está
relacionado com o uso racional de medicamentos e a implementação
de medidas efetivas de melhoria da situação sanitária da granja.
Neste sentido, são
ferramentas para o controle do desenvolvimento da resistência o controle
sanitário da granja, com exames bacteriológicos rotineiros e a análise dos
riscos clínico e epidemiológico, bem como melhorias nas práticas de limpeza e
desinfecção e a adoção de programas vacinais.
Quando da adoção de tratamentos antibióticos,
eles devem ser rápidos, a fim de limitar o desenvolvimento bacteriano,
respeitando doses e tempo de administração de cada princípio ativo.
Os principais desafios entéricos na fase
de creche
As doenças entéricas representam um problema
importante na suinocultura tecnificada, devido às grandes perdas econômicas
associadas com estas patologias. Os problemas decorrentes das diarreias em suínos são consequências
dos gastos com antibióticos, aumento da mortalidade, necessidade de manejo,
cuidados com os animais doentes e conversão alimentar inadequada (ZLOTOWSKI et al,
2008).
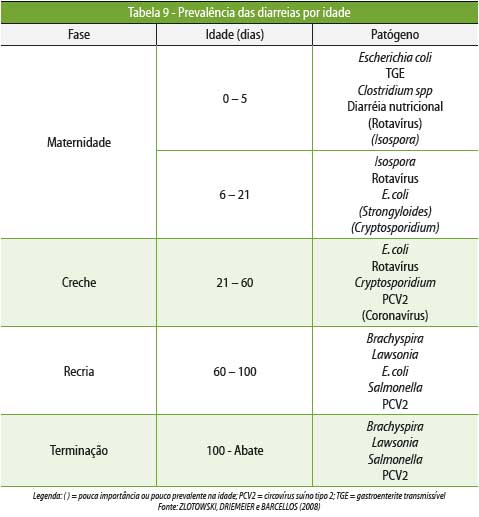
A Tabela 9 apresenta as causas de diarreias dos suínos e a fase em que ocorrem mais frequentemente.
Especificamente na fase de creche, a E. coli mantém como um
importante agente causador de enterite. Sua infecção é de difícil controle
devido à elevada capacidade deste agente em desenvolver e disseminar mecanismos
de resistência aos antimicrobianos utilizados no tratamento da doença.
BACCARO et
al (2002), estudando 600 amostras de E. coli isoladas de fezes de 100
leitões lactentes, com diarreia e idade variando
entre 5 e 30 dias, demonstraram que todas as amostras estudadas apresentaram
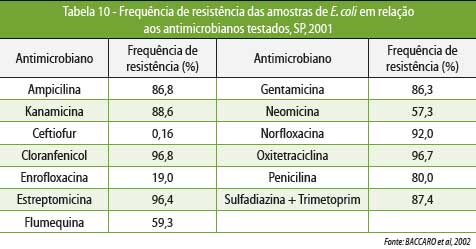
resistência a pelo menos 5 dos 13 antimicrobianos testados. A Tabela 10 mostra
a frequência de resistência observada nesse trabalho.
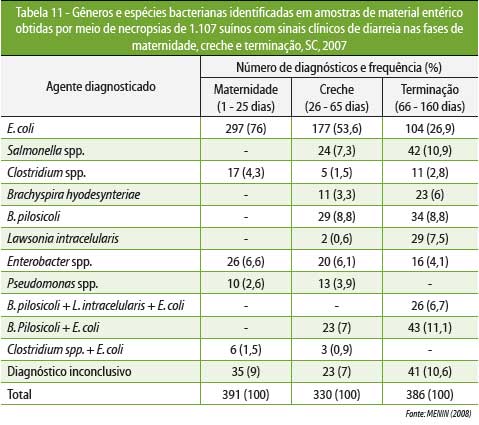
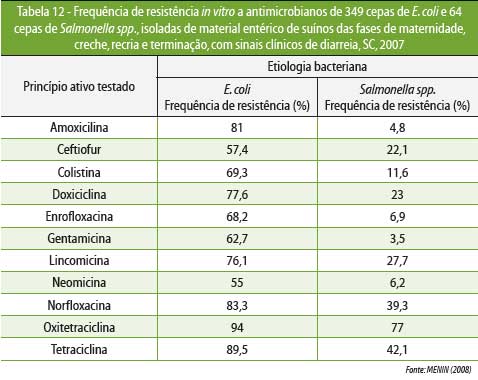
MENIN et
al (2008) determinaram os agentes bacterianos
associados com ocorrência de diarreias em suínos, em
diferentes faixas etárias, em Santa Catarina (Tabela 11), e também verificaram
o perfil de resistência de E. coli
e Salmonella spp. frente aos principais antimicrobianos utilizados em granjas
de suínos (Tabela 12).
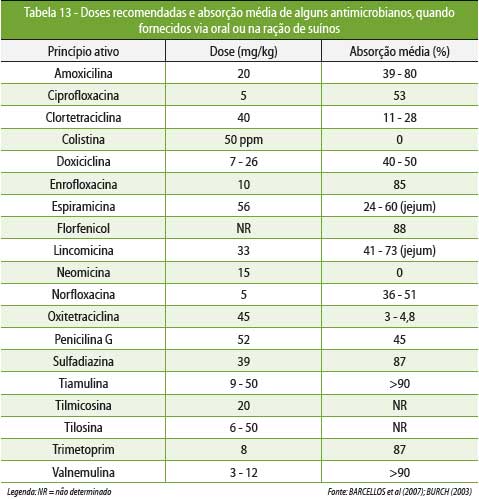
A Tabela 13 relaciona doses preconizadas e
absorção média de alguns antimicrobianos.
Independentemente da fase e, como já mencionado
anteriormente, as medidas de controle, tratamento e prevenção de doenças devem
estar relacionadas com o uso racional dos antibióticos, associadas às boas
práticas de limpeza e desinfecção, programas de vacinação adequados aos
desafios da granja e monitoramentos frequentes do
status sanitários da granja.
Possíveis causas de falha no tratamento
antibiótico
A função do médico-veterinário na assistência à
granja não pode se limitar somente à prescrição do tratamento. Cabe a ele,
também, determinar possíveis causas do insucesso do tratamento. Apesar de
muitas vezes atribuir-se a culpa da falha no tratamento antibiótico à
resistência bacteriana, há várias outras possíveis causas que devem ser
consideradas.
Entre as possíveis causas que levam ao insucesso
de um tratamento antibiótico, estão incluídas:
- Diagnóstico incorreto ou
incompleto
- Erros relacionados à
etiologia da doença: causa não infecciosa, outro agente infeccioso,
etiologia multifatorial;
- Interpretação incorreta do
antibiograma (Tabela 8).
- Implementação
incorreta do tratamento antibiótico
- Erro de dosagem;
- Instabilidade do
tratamento;
- Problemas de mistura ou
solubilização do medicamento;
- Consumo insuficiente.
- Ineficácia do antibiótico
no animal
- Antibiótico não indicado
para o microrganismo;
- Iteração medicamentosa;
- O antibiótico não atinge o
órgão-alvo;
- CIM muito alta e/ou
concentração do antibiótico muito baixa;
- Imunossupressão.
As causas de falha nos tratamentos podem estar
relacionadas com questões clínicas, bacteriológicas e até econômicas. É
fundamental que o médico-veterinário e os profissionais envolvidos estejam
atentos a possíveis causas de insucesso nos tratamentos.
Conclusão
O uso de antibióticos na produção animal sofrerá
cada vez mais pressão da opinião pública, exigindo que órgãos como o Ministério
da Agricultura sejam mais exigentes no sentido de limitar e controlar o uso
deste tipo de medicamento.
Além disso, a própria pressão decorrente da
resistência bacteriana exigirá mais critério no uso de programas antibióticos
por parte de médicos-veterinários, produtores e empresas.
No entanto, o uso dos antimicrobianos sempre
existirá e será necessário para garantir o sucesso na produção animal.
Por tanto, o uso racional de antibióticos,
vacinas, programas de limpeza e vacinação e controles sanitários fazem-se cada
vez mais necessários e indispensáveis.
